Ciclo Otto: fasi, rendimento, rapporto di compressione
Il ciclo Otto dal nome dell’ingegnere tedesco Nicolaus Otto è un ciclo impiegato nei motori a combustione interna come il motore a benzina in cui avviene la conversione di energia chimica posseduta da una miscela aria-benzina in lavoro meccanico.
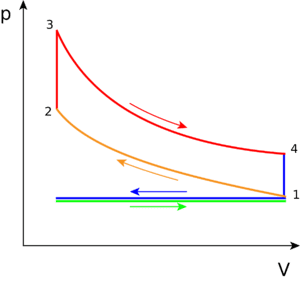
Nel ciclo Otto dopo che è avvenuta l’aspirazione della miscela aria-benzina essa viene compressa (1→2) con conseguente aumento della pressione e della temperatura. Segue la fase di combustione (2→3) che comporta un ulteriore aumento di pressione e temperatura e il volume rimane costante. Avviene poi l’espansione (3→4) del gas nel cilindro ed infine lo scarico dei gas (4→1). Questo ciclo può essere rappresentato in un diagramma pressione-Volume:
In termini generali, il ciclo Otto è un ciclo termodinamico che descrive i processi che agiscono su una massa di gas intrappolata durante i quattro tempi di un tipico motore a combustione interna. Nel ciclo Otto l’aria è considerata come il fluido di lavoro che si comporta come un gas perfetto e il calore specifico ha un valore costante
Fasi
| Cambiamento di stato | Fasi del ciclo Otto |
| A → B | Fase di compressione. Compressione adiabatica della miscela aria-benzina nel cilindro |
| B → C | Combustione della miscela aria-benzina compressa |
| C → D | Espansione adiabatica dei gas nel cilindro |
| D → A | Scarico dei gas esausti |
Rendimento di un ciclo Otto ideale
Il rendimento di una macchina termica è data da:
η = lavoro effettuato/ calore assorbito
indicando con QH il calore assorbito e con QL il calore ceduto si ha:
η = QH+ QL / QH = 1 + (QL / QH) (1)
Se si assume per convenzione che la variazione di calore è positiva se il calore fluisce all’interno del motore QL è negativo. La fase in cui il calore è assorbito durante la combustione si verifica quando si accende la scintilla a volume costante. Il calore assorbito può essere correlato alla variazione di temperatura dallo stato B allo stato C tramite la relazione:
QH = QBC = ΔU(BC) = ∫ CvdT = Cv(TC – TB)
Essendo TB e TC i limiti di integrazione.
Il calore rilasciato se il gas si comporta da gas perfetto con calore specifico costante è dato da:
QL = QDA = ΔU(DA) = Cv(TA – TD)
Sostituendo i valori ricavati nella (1) si ha:
η = 1 – TD – TA/ TC – TB
tale espressione può essere semplificata tenendo conto del fatto che i processi A → B e C → D sono isoentropici:
TDVAγ-1 = TCVBγ-1
TAVAγ-1 = TBVBγ-1
Da cui si ha:
(TD – TA) VAγ-1 = (TC – TB) VBγ-1
e raggruppando:
TD – TA / TC – TB = (VB/VA)γ-1
Il rapporto VA/VB è detto rapporto di compressione ed è indicato con r. Pertanto in termini di rapporto di compressione il rendimento di un ciclo di Otto ideale è dato da:
ηOtto = 1 – 1/( VA/VB) γ-1 = 1 – 1/r γ-1
Rapporto di compressione
Il rendimento di un ciclo Otto ideale è rappresentato come una funzione del rapporto di compressione. Esso è la caratteristica chiave di molti motori a combustione interna. Nella e determina l’efficienza termica del ciclo termodinamico utilizzato del motore a combustione.

In figura è rappresentata l’efficienza del ciclo Otto in funzione del rapporto di compressione
Quando il rapporto di compressione r aumenta si ha un aumento anche di ηOtto. Tuttavia se r è molto alto allora la miscela aria-benzina dà luogo alla combustione anche in assenza della scintilla.



