Coca Cola: determinazione di acido fosforico, punti equivalenti
La Coca Cola è la bibita analcolica più famosa e diffusa nel mondo che con campagne pubblicitarie sempre mirate e innovative ha conquistato un pubblico giovane e meno giovane.
Uno dei componenti della Coca Cola è l’acido fosforico sulla cui presenza è aperto un ampio dibattito in relazione ai danni che esso può provocare.
Per determinare la concentrazione dell’acido si può procedere con una titolazione titolazione acido-base.
Nella Coca Cola, oltre all’acido fosforico è presente anche l’acido carbonico proveniente dalla dissoluzione dell’anidride carbonica in acqua. Per far avvenire la decarbonatazione occorre allontanare l’acido carbonico ponendo in un becker, coperto da un vetrino da orologio in modo da evitare che l’anidride carbonica presente nell’aria si solubilizzi nel campione, la Coca Cola e portando a leggera ebollizione per circa 20 minuti.
Si fa raffreddare e nel campione è presente solo l’acido fosforico che può essere determinato tramite una titolazione usando idrossido di sodio preventivamente standardizzato con potassio ftalato acido.

Se si dovesse titolare l’acido fosforico in una soluzione la titolazione potrebbe essere effettuata con due opportuni indicatori, tuttavia, a causa della colorazione della Coca Cola che ne maschera il viraggio si usa un elettrodo a vetro che è il tipo di sonda maggiormente usato per la misura del pH di soluzioni acquose tramite il pH-metro.
Equilibri
L’acido fosforico è un acido triprotico e quindi è soggetto a tre equilibri di dissociazione:
H3PO4 + H2O ⇌ H2PO4– + H3O+ Ka1 = 7.5 ∙ 10-3
H2PO4– + H2O ⇌ HPO42- + H3O+ Ka2 = 6.2 ∙ 10-8
HPO42- + H2O ⇌ PO43- + H3O+ Ka3 = 2.2 ∙ 10-13
Punti equivalenti nella titolazione della Coca Cola
Dalla titolazione si hanno 3 punti equivalenti corrispondenti a:
H3PO4 + OH– ⇌ H2PO4– + H2O
H2PO4– + OH– ⇌ HPO42 + H2O
HPO42 + OH– ⇌ PO43 + H2O
Tuttavia il terzo punto equivalente non è rilevabile in quanto il valore della Ka3 è molto vicino al valore della costante di dissociazione dell’acqua Kw che è pari a 10-14 e ciò implica che lo ione fosfato compete con lo ione OH–.
La curva relativa alla titolazione dell’acido fosforico con NaOH è rappresentata in figura:
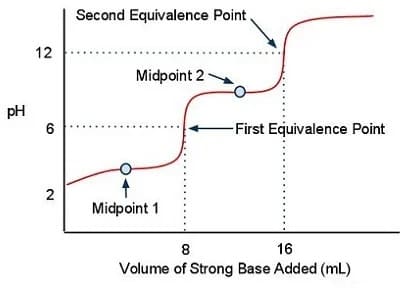
Un volume noto di Coca Cola di 5.0 mL può essere titolato con NaOH 0.0100 M. Si costruisce la curva relativa alla titolazione riportando in ascisse il volume di NaOH e in ordinate il relativo pH.

Dal grafico si rilevano i volumi di NaOH necessari per raggiungere il primo e il secondo punto equivalente esaminando dalla tabella dei dati quando avviene la maggiore variazione di pH a seguito di aggiunta di NaOH assicurandosi che a tale valore corrisponde, nel grafico, la massima pendenza. Il punto di equivalenza corrisponde al punto centrale del “salto” nella curva di titolazione. Utilizzare lo stesso metodo per determinare il secondo punto equivalente e calcolare la molarità dell’acido fosforico.



