I processi chimici della fotografia si fondano sul fatto che la luce, o meglio l’insieme di onde di varia lunghezza d’onda o frequenza che la costituiscono, è capace di modificare le molecole di varie sostanze che perciò vengono dette fotosensibili.
Storia
Fin dal Medioevo, gli alchimisti, studiavano i composti che viravano se esposti alla luce. Nel ‘700 gli scienziati Shultze e Wedgwood apportarono importanti sviluppi nel campo. Durante alcuni esperimenti con carbonato di calcio, acqua regia, acido nitrico e argento, fu scoperto che il composto ottenuto, fondamentalmente cloruro di argento, reagiva alla luce cambiando colore.
Furono ripetuti esperimenti riempiendo una bottiglia di vetro con i reagenti, Si notò che i prodotti di reazione cambiavano colore solo nel lato illuminato. A tale sostanza fu dato il nome di scotophorus, portatrice di tenebre. Gli studi compiuti, provocarono fermento nel mondo scientifico, ma solo verso la fine del 1700 l’inglese Thomas Wedgwood sperimentò l’utilizzo del nitrato di argento immergendovi dei fogli di carta che espose alla luce, dopo avervi deposto degli oggetti.
Si accorse che, dove la luce colpiva il foglio, la sostanza si anneriva, mentre rimaneva chiara nelle zone coperte dagli oggetti. Purtroppo queste immagini non si stabilizzavano e perdevano rapidamente contrasto se mantenute alla luce.
Camera oscura
Successivamente Joseph Nicephore Niepce si interessò al fenomeno e approfondì gli studi alla ricerca di una sostanza che potesse impressionarsi alla luce e che mantenesse il risultato nel tempo. Utilizzò un foglio di carta bagnato di cloruro di argento esponendo all’interno di una piccola camera oscura. L’immagine apparì invertita, con gli oggetti bianchi sul fondo nero.
Questo negativo non soddisfò Niepce, che proseguì la ricerca di un procedimento per ottenere direttamente il positivo. Scoprì che il bitume giudaico era sensibile alla luce e lo utilizzò nel 1822 per produrre delle copie di un’incisione. Il bitume di Giudea è un tipo di asfalto normalmente solubile in olio di lavanda e, una volta esposto alla luce indurisce. Niepce cosparse una lastra di peltro con questa sostanza e vi sovrappose l’incisione.
Dove la luce riuscì a raggiungere la lastra di peltro attraverso le zone chiare dell’incisione, si ebbe una sensibilizzazione del bitume che si indurì e non poté essere eliminato dal successivo lavaggio con olio di lavanda. La superficie rimasta scoperta venne scavata con acquaforte e la lastra finale poté essere utilizzata per la stampa.
Storia
Nel 1837 Daguerre utilizzò una lastra di rame con applicata un sottile foglio di argento che, posta sopra i vapori di iodio reagiva formando ioduro d’argento. Seguì l’esposizione alla camera oscura dove la luce trasformava lo ione argento in argento metallico. L’immagine non risultava visibile fino alla esposizione a vapori di mercurio. Un bagno in una soluzione di sale comune fissava, sia pur non stabilmente, l’immagine.
Il processo destò molto scalpore e si diffuse in tutta Europa diventando il principale metodo per ottenere fotografie. Fu solo nella seconda metà dell’Ottocento che Fox Talbot perseguì l’obiettivo di ottenere una fotografia come prodotto non più generato dalla mano dell’uomo, bensì grazie all’impiego della tecnologia. L’obiettivo delle ricerche di Talbot divenne quindi quello di riuscire a ottenere delle immagini foto-chimiche.
Egli, nel libro The pencil of the nature, pubblicò le sue ricerche corredando il testo con numerose fotografie. Talbot mise a punto un procedimento fotografico che permetteva la riproduzione delle immagini con il metodo negativo/positivo tramite il quale si potevano ottenere molte copie della medesima posa. Sia il negativo che il positivo erano costituiti da una carta impregnata di cloruro di argento.
La strada della fotografia era aperta ed ebbe grande diffusione in tutto il mondo.
Processi
Da allora molto tempo è passato, ma ancora oggi, i processi chimici , si basano su quattro tappe fondamentali:
1) Fotoreazione iniziale
2) Sviluppo
3) Fissaggio
4) Stampa
Il supporto per conservare le immagini riprese con la macchina fotografica a pellicola è la pellicola fotografica che è costruita a strati: il supporto base è costituito da un sottile nastro di materiale plastico su cui è applicato uno strato di gelatina che porta in sospensione dei piccoli cristalli di AgBr.
La gelatina usata in fotografia si ottiene tramite la degradazione del collagene, proteina a struttura lineare molto diffusa nel mondo animale. I cristalli di AgBr, detti grani, si preparano trattando una soluzione di AgNO3 con KBr; si ottiene, tramite una reazione di precipitazione AgBr che, data la sua scarsa solubilità precipita in cristallini.
La grandezza dei grani dipende dal tempo di riposo. Se questo è breve si ottengono grani di piccole dimensioni, se è prolungato si ottengono grani più grossi. Poiché la dimensione dei grani ha notevole importanza nel processo fotografico, questa reazione deve essere condotta con particolare cura.
I grani sono poi mischiati a gelatina fusa: si forma una sospensione, detta comunemente emulsione sensibile, che si applica in strato sottile sul supporto.
Reazioni
Una radiazione luminosa di giusta frequenza che colpisca i grani di AgBr dà l’avvio a una serie di reazioni concatenate che avvengono ad opera della luce dette fotochimiche. Avvengono quindi i seguenti processi chimici:
Ag+ Br– → Ag+ + Bro + e–
Ag+ + e– → Ago
Ago + Ag+ = Ag2+ + e– → Ag2o
Ag2o + Ag2+ → Ag3+ + e– →Ag3o
Ag3+ +Ag = Ag4+ + e– → Ag4o
Nel reticolo cristallino di AgBr si formano alcuni atomi di Ag neutro ( Ago) che si inseriscono tra le maglie, man mano che la luce libera gli elettroni dal Br– del grano. Sono necessari almeno 4 atomi di Ag perché sia possibile lo sviluppo. Gli aggregati di atomi di Ag+ costituiscono l’immagine latente. Gli atomi di Bro per la configurazione elettronica non completa ( p5) , sono pronti a catturare un elettrone e ad aggregarsi agli ioni Ag+
Ag+ + Bro+ e– → AgBr
Reazioni di Bro
In definitiva tendono a impedire la formazione dell’immagine latente, o a distruggere l’immagine latente già formata, riducendo la grandezza degli aggregati di atomi di Ag:
Bro + Ag4o (grano sviluppabile) → Ag3o (grano non sviluppabile) + Ag+ Bro + e–
Il Bro, per la sua alta elettronegatività, si comporta come una buca positiva, richiamando l’elettrone dell’Ago e accelerando la reazione di demolizione dei nuclei di Ago; anche dagli ioni Br– sono richiamati elettroni e la buca si sposta in seno alla compagine AgBr-Ago. per eliminare tale inconveniente si aggiungono all’emulsione sensibile delle sostanze dette sensibilizzanti che non permettono la distruzione dell’immagine latente, e addirittura ne permettono il formarsi. La scoperta dei sensibilizzanti fu casuale (Sheppard , 1925). Avvenne quando, dopo aver usato una gelatina che conteneva impurezze di zolfo, ci si accorse che l’immagine latente non era obliterata.
Uso del solfuro di argento
Oggi, all’emulsione gelatina-bromuro di argento si aggiunge anche solfuro di argento: gli atomi di Bro che si comportano da buca positiva mobile catturano selettivamente gli elettroni dallo ione S2- , senza impedire la formazione di Ago e senza demolire gli aggruppamenti di atomi di Ag già formati:
2 Bro + Ag2S → 2 Ag+Br– + S
Quindi Ag2S rende davvero più veloce la reazione e accresce la sensibilità dell’emulsione. Anche la dimensione dei grani di AgBr influenza la sensibilità della pellicola. Se i grani sono grandi, cioè formati da molte unità di AgBr, la possibilità di fotoreazione è superiore a quella di grani piccolissimi. Sono infatti necessari almeno 4 Ag per dare l’avvio alla reazione a catena. Se però i grani sono molto grandi, un gruppo di 4 Ag non è più sufficiente per la propagazione della reazione in tutto il grano. Deve esserci un numero superiore di inneschi, e quindi la reazione rallentata determina una minore sensibilità.
Sviluppo
Un unico fotone che colpisce un grano di AgBr produce la formazione di almeno 4 atomi di argento ridotto. Con l’impiego di sostanze riducenti appropriate si ha la possibilità di trasformare velocemente una enorme quantità di ioni argento in argento elementare specialmente se nei grani si sono già formati germi di atomi neutri di Ag. I grani che non ne contengono rimangono inalterati. La pellicola impressionata dalla luce è immessa in un bagno di sviluppo nel quale agisce da riducente un rivelatore.
La sostanza riducente più comunemente usata per foto in bianco e nero è una soluzione di idrochinone; un rivelatore tipo contiene una o due molecole riducenti, un antiossidante e un tampone alcalino che mantenga costante il progredire della reazione regolando il pH.
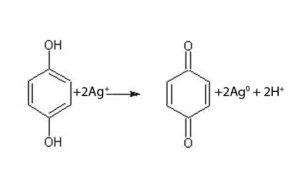 Per impedire il retrocedere della reazione di equilibrio si tratta con Na2SO3: la reazione produce ioni OH- che catturano ioni H+ derivati dall’azione precedente, impedendone il regredire. Il borace in soluzione agisce come tampone assorbendo H+ formatosi dalla precedente reazione:
Per impedire il retrocedere della reazione di equilibrio si tratta con Na2SO3: la reazione produce ioni OH- che catturano ioni H+ derivati dall’azione precedente, impedendone il regredire. Il borace in soluzione agisce come tampone assorbendo H+ formatosi dalla precedente reazione:
Na2B4O7 + 10 H2O → 2 H3BO3 + 2 Na+ + 2 B(OH)4– + 3 H2O
H+ + B(OH)4– →B(OH)3 + H2O
La reazione di sviluppo è strettamente collegata alla temperatura e al tempo di immersione. La permanenza di una pellicola nel bagno per un tempo prolungato, a temperatura superiore al dovuto, provoca un annerimento totale. Un bagno di arresto in soluzione di acido acetico conclude il processo di sviluppo perché gli ioni H+ che abbassano il pH impediscono all’idrochinone di trasformarsi in chinone.
Fissaggio
In una pellicola impressionata, solo nei grani esposti alla luce, si sono formati atomi neutri di argento. Il rivelatore ha poi accentuato la riduzione permettendo la formazione di nuovi aggregati di Ago che si propagano da quelli iniziali.
Se dalla pellicola già trattata non è eliminato l’Ag+ Br– residuo, c’è il rischio che, a causa di radiazioni luminose o di qualsiasi agente riducente, anche questo reagisca producendo Ago e faccia quindi annerire la pellicola. Si dice fissaggio il trattamento per mezzo del quale si lava via solo lo ione Ag+ non trasformato, in modo che sulla pellicola rimanga solo l’Ag ridotto.
Il fissatore è Na2S2O3 tiosolfato di sodio, capace di legarsi con AgBr formando un complesso solubile che è portato via attraverso numerosi lavaggi della pellicola.
AgBr (solido, insolubile) + 2 S2O32- → Ag(S2O3)23- ( complesso solubile) + Br–
Sulla pellicola resta solo Ago, mentre Ag+ passa nelle acque di lavaggio dalle quali può anche essere recuperato, dato che sulla pellicola ne resta il 20-40%.
Stampa
Sulla pellicola sviluppata, fissata e sottoposta a lavaggio rimangono delle zone scure, dovute alla formazione di Ago, e delle zone chiare, quelle dalle quali l’AgBr non trasformato è eliminato per mezzo del fissaggio. La stampa si ottiene investendo il negativo con un fascio di luce intensa, che attraversandolo deve colpire una carta sensibile. Anche la carta sensibile contiene grani di AgBr (o di AgCl più stabile), più piccoli di quelli della pellicola, quindi molto meno reattivi. Le carte sensibili sono perciò più facili da trattare di quanto lo sia una pellicola non sviluppata, perché i tempi di reazione sono più lunghi.
