L’ossido di vanadio (V), pentossido di bivanadio o anidride vanadica è un solido di colore giallo-arancio scarsamente solubile in acqua avente formula V2O5. Si trova in natura come il raro minerale shcherbinaite.
Costituisce una fonte di vanadio termicamente stabile altamente insolubile e quindi adatto per applicazioni in vetro, ottica e ceramica.
L’uso maggiore dell’ossido di vanadio (V) risiede nella sua attività catalitica nella sintesi dell’acido solforico. Esso infatti catalizza la trasformazione dell’anidride solforosa in anidride solforica
Nella sua struttura ciascun atomo di vanadio è legato tramite doppio legame a due atomi di ossigeno ed è presente un atomo di ossigeno che è legato ad entrambi gli atomi di vanadio.
Reazioni
L’ossido di vanadio è un ossido anfotero pertanto reagisce con le basi secondo la reazione:
V2O5+ 6 OH– → 2 VO43- + 3 H2O
per dare il vanadato
Mentre reagisce con gli acidi non riducenti secondo la reazione:
V2O5 + 6 H+ → 2 VO2+ + H2O
per dare il diossovanadio.
L’ossido di vanadio ossida l’acido cloridrico a cloro secondo la reazione:
V2O5 + 6 HCl → 2 VOCl2 + Cl2 + 3 H2O
In presenza di riducenti come il calcio l’ossido di vanadio (V) si riduce a vanadio metallico:
V2O5 + 5 Ca → 2 V + 5 CaO
Sintesi
L’ossido di vanadio si ottiene per decomposizione termica del metavanadato di ammonio secondo la reazione:
2 NH4VO3 → V2O5 + 2 NH3 + H2O
Usi
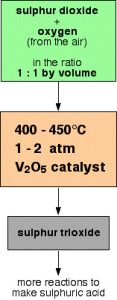
Il pentossido di vanadio è utilizzato in molti processi industriali quale catalizzatore.
Nel processo di contatto per la produzione di acido solforico viene usato per ossidare l’anidride solforosa a anidride solforica:
2 SO2 + O2 → 2 SO3
Viene anche usato nell’ossidazione dell’etanolo a etanale e nella produzione di anidride ftalica, acido ossalico e altri prodotti di interesse industriale.
Le aldeidi danno luogo a una esterificazione catalitica ossidativa in presenza di ossido di vanadio e perossido di idrogeno. Tale metodo è molto efficace in quanto richiede condizioni blande e avviene in tempi brevi con bassi costi, alta resa e facile isolamento dei prodotti.

